本网讯(生命科学与医学工程学院洪靖君)近日,我校生命科学与医学工程学院洪靖君教授课题组在染色质重塑复合物亚基YL1识别组蛋白变体H2A.Z的分子机制研究方面取得新进展。研究团队成功解析了人源SRCAP染色质重塑复合物亚基YL1与组蛋白变体H2A.Z/H2B二聚体复合物的高分辨率晶体结构,揭示了YL1特异性识别H2A.Z的精确分子机制。相关成果以“Structural Insights into Specific Recognition of the Histone Variant H2A.Z by the YL1 Subunit of SRCAP Chromatin-remodeling Complex”(DOI: 10.1016/j.jbc.2026.111294)为题,在线发表在国际生物化学与分子生物学领域的权威期刊《Journal of Biological Chemistry》。
染色质的基本单元是核小体,组蛋白变体H2A.Z替换常规组蛋白H2A是调控基因转录动态变化的关键步骤之一。这一过程由染色质重塑复合物如SRCAP执行,其亚基YL1负责识别并招募H2A.Z/H2B二聚体。尽管此前已有果蝇和人的YL1与H2A.Z/H2B复合物的结构报道,但两者之间存在显著差异,导致领域内对YL1如何招募H2A.Z/H2B的精确机制存在困惑。
为解决这一关键问题,洪靖君教授课题组开展了深入研究。通过共表达与纯化技术,获得了人源YL1-Z结构域(N端8-73位氨基酸)与单链连接的H2B-H2A.Z(hTBZ)复合物,并成功解析了其高达2.01 Å分辨率的晶体结构。结构分析显示,YL1-Z结构域由一个α螺旋和一个较长的loop环组成,其通过疏水相互作用和静电相互作用与H2A.Z/H2B二聚体紧密结合。MBP-pulldown和等温滴定量热法(ITC)实验进一步验证了结构中关键残基在特异性识别中的作用。值得注意的是,该研究获得的人源YL1-Z/H2A.Z/H2B复合物结构与之前报道的果蝇YL1与H2A.Z/H2B复合物结构高度相似,这表明YL1识别H2A.Z/H2B的结构机制在进化上是保守的。这一高分辨率结构为理解染色质重塑复合物如何特异性识别组蛋白变体提供了最直接、最可靠的依据。
该研究成果不仅阐明了领域内关于YL1识别H2A.Z机制的疑问,也为后续的功能研究和靶向药物设计奠定了坚实的结构基础。博士研究生谭万森为论文第一作者,洪靖君教授为通讯作者兼共同第一作者,硕士研究生刘玥参与相关工作,安徽大学为论文的唯一单位。该研究得到了国家自然科学基金的资助。晶体数据收集得到了安徽大学王明珠副研究员及中国科学技术大学金腾川教授团队的帮助,模型构建中感谢江健生博士提出中肯的建议。
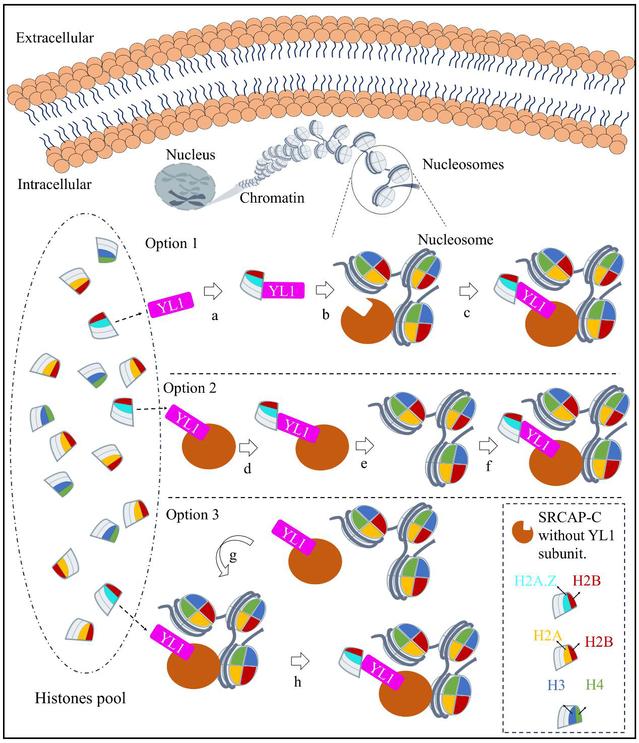
图 YL1亚基招募H2A.Z/H2B可能的分子机制图
洪靖君教授长期致力于染色质重塑过程中组蛋白变体特异性识别的结构生物学基础研究,洪靖君教授在酵母模型中首次揭示了SWR1复合物催化亚基Swr1如何特异性识别H2A.Z/H2B二聚体(成果发表于《Molecular Cell》),而后从酵母拓展至人源,聚焦于人源SRCAP复合物(酵母SWR1的同源复合物)中的YL1亚基,系统地阐明了从酵母到人类,染色质重塑复合物识别H2A.Z的保守结构基础。




