本网讯(生命科学与医学工程学院王丽莉)近日,我校生命科学与医学工程学院杨兴元教授团队在国际氧化还原生物学领域顶级期刊《Redox Biology》发表题为 “Acetyl-CoA acyltransferase 2 palmitoylation drives liver fibrosis by inducing hepatic stellate cell ferroptosis” (DOI:10.1016/j.redox.2026.104035)的研究论文。该研究首次揭示了脂肪酸β-氧化关键酶 ACAA2 的棕榈酰化修饰在肝纤维化发生发展中的关键作用,阐明了其通过调控肝星状细胞(HSCs)铁死亡驱动肝纤维化的新机制,为理解代谢-氧化应激-铁死亡轴在慢性肝病中的作用提供了重要理论依据。博士研究生韩健雄与颜忠康为论文共同第一作者,杨兴元教授、汪菲菲讲师和王丽莉副教授为共同通讯作者,安徽大学为第一署名单位。
肝纤维化是多种慢性肝病向肝硬化和肝细胞癌进展的共同病理基础,其核心事件是肝星状细胞的异常激活和持续性促纤维化反应。近年来,铁死亡(ferroptosis)作为一种依赖铁离子和脂质过氧化的程序性细胞死亡方式,被认为在肝脏疾病中具有双向调控作用。然而,代谢相关蛋白翻译后修饰如何精细调控 HSC 铁死亡及其在肝纤维化中的功能仍不清楚。
本研究通过人肝纤维化样本及多种小鼠肝纤维化模型发现,ACAA2 在纤维化肝组织中棕榈酰化水平显著升高,并主要定位于活化的肝星状细胞。机制研究进一步表明,ACAA2 的棕榈酰化增强其线粒体定位和脂肪酸氧化通量,导致线粒体氧化应激加剧、脂质过氧化积累及铁稳态失衡,从而显著提高 HSC 对铁死亡的敏感性。通过遗传学和药理学手段干预 ACAA2 棕榈酰化,可有效抑制 HSC 铁死亡并减轻肝纤维化程度。
进一步研究证实,ACAA2 棕榈酰化介导的代谢重编程与 GPX4 抑制、xCT 下调及铁负荷增加密切相关,三者共同构成驱动肝星状细胞铁死亡的关键分子网络。在动物体内实验中,肝特异性调控ACAA2 棕榈酰化显著影响肝纤维化进展,提示其在代谢相关肝病中的潜在干预价值。
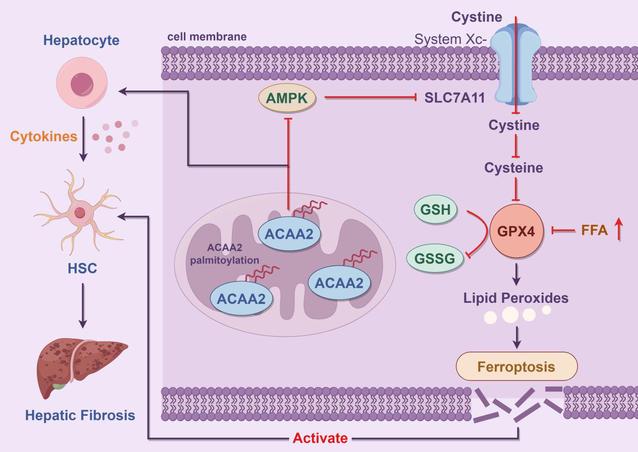
图 ACAA2通过铁死亡促进肝纤维化模式
本研究从蛋白质翻译后修饰的新角度,系统阐明了脂肪酸代谢、氧化还原稳态与铁死亡在肝纤维化中的交叉调控机制,不仅拓展了对ACAA2 生物学功能的认识,也为靶向铁死亡和代谢通路治疗肝纤维化提供了新的分子靶点和理论基础。
杨兴元教授团队长期致力于代谢与疾病的分子调控以及代谢微环境相关交叉学科的基础研究,近年来在《Bioresource Technol》、《Oncogene》、《J Biol Chem》发表了系列研究成果。该研究得到国家自然科学基金的资助,部分实验得到中国科技大学顾朋颖老师以及安徽医科大学何安元教授的大力支持。




