本网讯(生命科学与医学工程学院 高佳佳)近日,生命科学与医学工程学院葛宏华教授课题组在胞内致病菌与宿主相互作用机制研究方面取得最新进展,揭示了嗜肺军团菌效应蛋白Ceg10如何通过乙酰化修饰破坏宿主核糖体功能,抑制蛋白翻译并干扰细胞周期,从而促进细菌在宿主细胞内的增殖。相关成果以“Legionella effector Ceg10 acetylates RPS20 to inhibit host translation and induce cell cycle arrest”为题,发表于国际综合性学术期刊《美国国家科学院院刊》(PNAS,DOI: 10.1073/pnas.2517995123)。博士后高佳佳为论文的第一作者,博士研究生许雯雯为共同第一作者,葛宏华教授为通讯作者,硕士研究生周子怡、陆立新、青年教师王伟强和中山大学陆勇军教授、葛振煌副研究员参与了相关研究工作,安徽大学为第一作者和通讯作者的唯一单位。
嗜肺军团菌是一类可在巨噬细胞内生长并导致严重肺炎的胞内病原体,它通过分泌大量效应蛋白操控宿主细胞。本研究采用免疫共沉淀、体外Pull-down及蛋白质组学分析等,鉴定了效应蛋白Ceg10与宿主40S核糖体蛋白RPS20的直接相互作用。通过结构解析与生化实验,结合高分辨率质谱,确定了Ceg10是一类含有CHD motif的乙酰转移酶,可以对RPS20三个关键氨基酸位点进行乙酰化修饰,这些修饰破坏了RPS20与RPS29及18S rRNA的正常结合,从而阻碍了核糖体小亚基的装配。进一步研究显示,Ceg10的乙酰化活性导致宿主整体蛋白质合成速率显著降低;同时,Ceg10通过抑制Cyclin D1-CDK4/6-Rb轴的正常动态调控,使宿主细胞阻滞于G1/S期,从而影响细胞周期进程。研究还发现,Ceg10进入宿主细胞核需要核转运适配蛋白HEATR3的介导,这一发现为理解细菌效应蛋白如何劫持宿主核转运系统提供了新的证据。在细胞感染模型中,缺失Ceg10的军团菌在宿主细胞中显示出生长受限与毒力下降,而恢复表达Ceg10可完全补偿上述缺陷,表明其在感染早期阶段具有关键作用。
该研究从结构、生化功能到细胞与感染模型多层次地阐明了Ceg10的作用机制,揭示了嗜肺军团菌利用乙酰化修饰破坏宿主核糖体功能,并通过抑制蛋白翻译和扰乱细胞周期促进感染,这是一种与靶向翻译起始因子或延伸因子的经典翻译抑制模式截然不同的新策略,拓展了我们对病原体操控宿主翻译机制的理解。该成果为深入理解胞内致病菌的感染策略提供了新的理论依据,也为未来抗感染治疗靶点的开发提供了潜在方向。
|
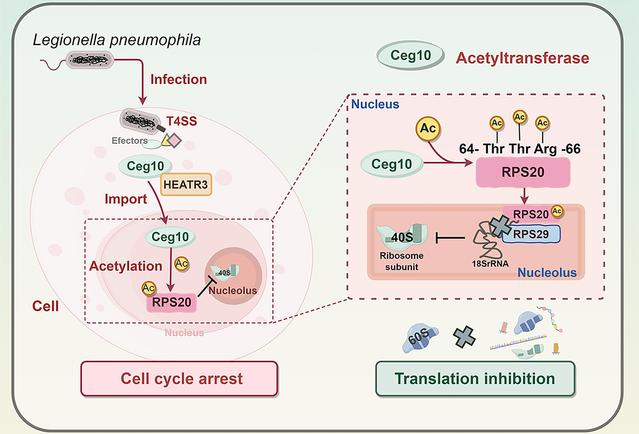
图 效应蛋白Ceg10抑制宿主蛋白翻译和阻滞细胞周期模式图
葛宏华教授团队长期致力于微生物–宿主互作机制与细菌信号调控的分子基础研究,相关成果在2025年相继发表于《Advanced Science》《Microbiol Spectr》《mBio》《Int J Biol Macromol》和《Science Advances》等期刊。该研究得到国家自然科学基金和中国博士后科学基金项目的资助,部分实验得到中国科学技术大学朱中良老师以及安徽大学王明珠副研究员的重要帮助。